心臓血管外科のご紹介
患者様の体に負担の少ない治療を提供します。
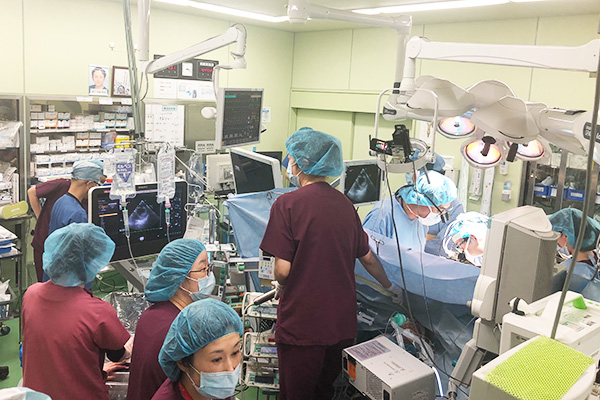
当科では、豊橋、名古屋両ハートセンターとの緊密な連携のもと、国内有数の経験豊富な医師たちが、安全性の高い医療の提供に努めています。
特に”できるだけ体への負担が少ない治療”を心がけております。例えば冠動脈疾患の手術では、術中に人工心肺を使わない”オフポンプ”による血行再建や、メスによる傷をできる限り小さくする処置に努めております。
また、安心して治療を受けていただけるよう、術前・術中・術後には患者様とご家族の皆様に十分な説明をさせていただいております。

断らない、安心・安全の医療体制に努めています。
心臓疾患は一刻を争う場合が多いため、当科では”断らない、安心・安全の医療”をモットーとしています。
緊急の場合は、直接お電話いただけば、いつでも対応させていただきます。
患者様へ
ご自分で外来にお越しになれる場合 予約なしでも大丈夫です。診察は月曜日〜金曜日の午前中に行っております。 なお、事前予約も可能ですので、電話もしくはFAXでご連絡ください。
緊急の場合、いつでも心臓血管外科の担当医師が対応いたします。代表番号 058-277-2277にお電話ください。
連携先の先生方へ
病診連携室へ通常の流れでも結構ですし、直接外科医師を呼び出ししていただき御相談いただいても結構です。
医療相談(セカンドオピニオン)について
当院心臓外科では、他院にて勧められた手術治療や方針に不安を感じられている患者さんに対するご相談も承っています。診療情報提供があればスムースですが、主治医にその旨を言い出しにくい場合には、まず当院に電話をして「治療方針の相談目的」で外来予約をお取りくださって結構です。お話を伺った上で必要に応じて簡単な検査をすることはありますが、できる限り患者さんに負担や不安のないように専門医としての見解をお伝えしていますので、お気軽にご相談ください。
代表番号 058-277-2277
スタッフ紹介
非常勤医師
病気と治療方法
<虚血性心疾患(狭心症、心筋梗塞)>
心臓は全身に血液を送るポンプの役割をしています。
生命の維持には血液供給(酸素、栄養など)が必要ですが、心臓自身も血液の供給を受けなければ、ポンプ機能を維持できません。心臓自身に血液を供給する血管を“冠動脈”で、この血管が詰まったり(閉塞)、細くなること(狭窄)で血液の供給不足となった疾患を、虚血性心疾患と呼びます。
冠動脈が細くなって、心臓の筋肉(心筋)に十分な血液が供給されない状態を狭心症といいます。急に冠動脈が閉塞して、心筋に血液が供給されなくなる状態を心筋梗塞といい、心筋にダメージを与えるため、早期の血流再開が必要となります。
冠動脈に対する外科的手術を冠動脈バイパス術と言います。
詰まっている・もしくは狭くなっている冠動脈の更に下流に、新しい血管(グラフト)を吻合します。渋滞している道路の上に新しくバイパスの道路を作り、良好な流れを作ることで、血流が不足していた心筋に十分な血液を供給できるようになります。
グラフトには、胸の内側にある内胸動脈や、足にある大伏在静脈が多く使用されます。胃にある胃大網動脈や手の橈骨動脈を使用する場合もあります(図1)。
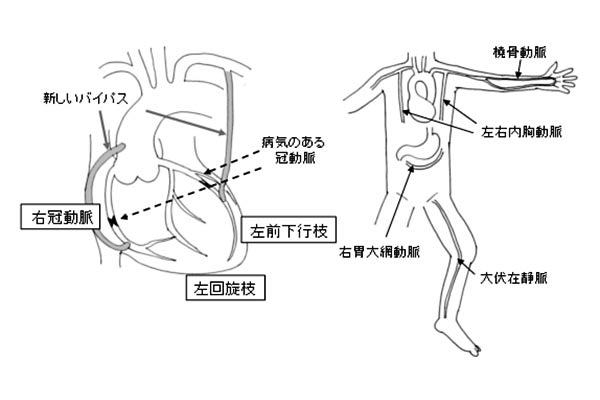
(図1)
また心臓は常に動いている臓器なので、心臓手術の多くは血液を全身に送るポンプ(人工心肺装置)を用いて心臓を停止して手術を行いますが、冠動脈バイパス術は人工心肺を使わないで手術することが可能です。
この術式は、オフポンプ(心拍動下)冠動脈バイパス術と呼ばれており、平成の天皇陛下が受けられた手術としてご存知の方も多いと思います。
*当科の特徴
術前に冠動脈の病気の重症度を評価して、カテーテル治療か冠動脈バイパス術かいずれが適しているかを内科医と外科医とで検討しています。
単独の冠動脈バイパス術では、心臓を停止することなく、オフポンプ(心拍動下)冠動脈バイパス術を基本術式としています。現在の人工心肺は非常に安全になっており過度に怖がる必要は無いですが、人工心肺を用いないことにより、人工心肺に伴う体の負担・合併症(肺障害、脳梗塞など)を更に減らすことができ、より安全にバイパス術を施行できると考えています。
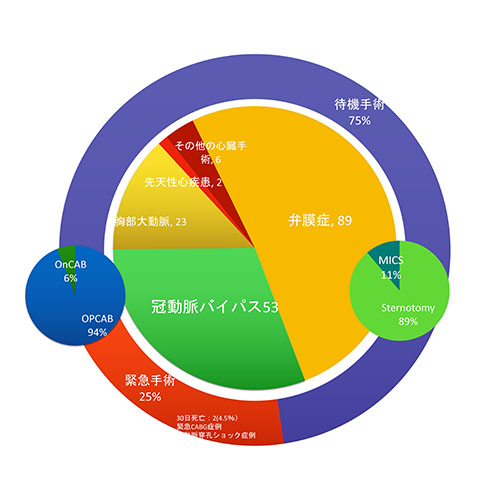
2020年1月から2021年12月の2年間で、冠動脈バイパス術の94%(112/119例)に人工心肺を用いず(オフポンプ)、心拍動下に行っております。
もちろん人工心肺を使用した方が安全に手術を行うことができる場合もあります。患者様の状況に応じて選択できることも重要であると考えています。
また、バイパスに用いる血管(グラフト)は、長期成績が良好である内胸動脈を両側とも用いることを原則としています。病変の血管の状態に応じてグラフトの選択を行いますが、長期成績の良好である動脈グラフトを優先して使用します。
吻合した血管は、手術中に血流計を用いて十分な血流が確保されているか確認します。安心して退院後の生活が送れるよう、術後1週間前後で退院前に造影検査(カテーテル・CT)で評価しております。
<心臓弁膜症>
心臓は全身に血液を送るポンプの役割をしています。
血液の循環を図2に示します。酸素を消費した血液(青矢印)は、心臓に戻って最初の部屋である右心房に帰り、右心室へ移動し、一旦心臓から出て肺に流れます。肺でガス交換が行われて酸素を多く含んだ血液(赤矢印)が心臓に戻り、左心房に入ります。その後左心室に血液が流れ、ここから全身に血液が押し出され、全身に血液が供給されます。

(図2)
血液は一方通行で効率よく流れていく必要があるため、心臓の4つの部屋の出口には前の部屋に逆流しないように一方弁がついています。
全身⇨右心房⇨三尖弁(さんせんべん)⇨右心室⇨肺動脈弁(はいどうみゃくべん)⇨肺⇨左心房⇨僧帽弁(そうぼうべん)⇨左心室⇨大動脈弁(だいどうみゃくべん)⇨全身、となります(図3)。
この弁に異常をきたすこと心臓弁膜症と言います。
弁が壊れて逆流している状態を閉鎖不全症、弁が硬くなって開きにくい状態を狭窄症と言います。疾患の呼び方は、心臓弁の種類と異常をきたした状態を組み合わせて呼びます。例えば僧帽弁が壊れて逆流している疾患は、“僧帽弁閉鎖不全症“、大動脈弁が硬くなって開きにくくなっている疾患は、”大動脈弁狭窄症“と言います。
病気の頻度が多いのは大動脈弁疾患と、ついで三尖弁疾患です。

(図3)
1.大動脈弁疾患
大動脈弁狭窄症と大動脈弁閉鎖不全症があります。これらに対する心臓手術は悪くなった自分の弁を取り除いた後、人工弁を用いて弁を置き換える手術(弁置換術)が主体です。
大動脈弁手術は多くは弁置換術が行われますが、弁形成術も行われるようになっています。自己の大動脈弁を修理して行う場合や、自己心膜を用いた形成術がありますが、大動脈弁形成術にはメリット・デメリットがありますので、形成術が適切かどうかは医師にご相談ください。
また大動脈弁狭窄症は、カテーテル治療(TAVI:経カテーテル的大動脈弁留置術)を行うことも可能です。カテーテルで治療を行う場合、原則は負担の少ない足の付け根(大腿動脈アプローチ)から行いますが、治療ができない場合は、外科的な技術を用いてカテーテル治療を行います(図4)。

(図4)
肩の血管から治療する方法(TS)、開胸して大動脈(DA)もしくは心臓の先端(TA)から治療する方法があります。
外科的治療を組み合わせることで、カテーテル治療を可能とします。
治療法の選択は患者様の状態などを考慮して行います。

(図5)
*当科の特徴
低侵襲心臓手術(MICS:ミックス)での弁置換術も可能です。また人工弁の選択も従来の生体弁、機械弁以外にスーチャレス弁(縫わない生体弁)の使用も可能です。
また大動脈弁狭窄症に対するカテーテル治療(TAVI)では、大腿動脈アプローチ以外のアプローチも選択でき、当科部長が指導医(プロクター)として全国の病院に安全な導入ができるように指導を行っております。当施設は岐阜県下唯一(東海地方では3施設のみ)である透析患者様に対するTAVIも施行可能です。
多くの治療選択肢は、様々状態の患者様に最適な治療が選択できると考えています。治療法にはメリット・デメリットがあります。遠慮なく相談してください。
2.僧帽弁疾患
僧帽弁狭窄症と僧帽弁閉鎖不全症があります。
僧帽弁狭窄症は、リウマチ熱や動脈硬化などが原因であることが多く、進行性であるため、悪くなった弁を取り除き、人工弁で置き換える(弁置換術)が主体となります。弁を残して治療する弁形成術が可能な場合もありますが、状態が限られます。
一方、僧帽弁自体が壊れて逆流している変性性僧帽弁閉鎖不全症(DMR)の治療の主体は、人工弁を用いず壊れた弁を修復して治療する弁形成術です。弁形成術は、自分の弁を用いて、壊れた部分を切り取って縫合修復する方法(切除縫合)や特殊な糸で弁の支えを行う方法(人工腱索)、拡大した弁の枠組みを小さくする方法(人工リングによる形成)を組み合わせて治療します(図6)。
弁形成術の有利な点は、機械弁を使用することで必要となる抗凝固薬(血液が固まりにくくなる薬)の内服を避けることができ、生体弁より長持ちし、さらに心機能の維持です。
また僧帽弁自体が壊れていないにもかかわらず、心筋梗塞などで左心室が悪くなることで二次的に僧帽弁閉鎖不全症が起こることがあります。これを機能性僧帽弁閉鎖不全症(FMR)と言います。治療法は、弁形成術、弁置換術、またカテーテル治療(MitraClip)かは、患者様の年齢や背景、合併症、他の心疾患の状況によって異なります。
*当科の特徴
僧帽弁閉鎖不全症に対する弁形成術を第一選択としており、複雑な病変(バーロー病など)に対する弁形成術も重症心不全を合併している場合を除き、積極的に行っております。
2020年1月から2021年12月までの2年間で、変性病変による僧帽弁閉鎖不全症(DMR)に対する僧帽弁手術は、97%で弁形成術を行っており、弁形成術は100%で完遂しております(弁形成術61例(術中弁置換術への移行なし)/弁置換術2例)。また3D内視鏡を用いて低侵襲心臓手術(MICS:ミックス)も積極的に行っております。3D内視鏡を用いることで、詳細に病変を把握し、3〜4cmの小さい傷で行うことが可能です。
機能性僧帽弁閉鎖不全症(FMR)に対しては、手術治療だけでなく、カテーテル治療(MitraClip)も選択肢の一つですので、患者様に最適な治療法を考えます。

(図6)
<人工弁>
心臓弁膜症の治療は、人工弁を使用して悪くなった弁を取り換えることが原則となります。
機械弁はパイロライトカーボンという素材でできており、耐久性が非常に高いのが長所です(図7)。
しかし異物である素材があるため血液が固まろうとして、血のかたまり(血栓)を形成することがあります。これを防ぐためにワーファリン*を飲まなくてはいけません。
ワーファリン*は血液を固まりにくくする薬(抗凝固薬)で、定期的に血液検査で効果を判定し、投与量を調整する必要があります。効き過ぎると出血しやすく、効いていないと血栓や塞栓症を起こすことがあります。
またビタミンKを含んだ食物摂取(納豆など)を食べるとワーファリンの効果が減弱します。
ワーファリンは胎児への影響があるため、妊娠出産の可能性がある方は内服できません。機械弁の短所はワーファリンが必要なことと考えます。
生体弁はウシの心膜やブタの大動脈弁を加工して作られた弁です(図8)。
生体の組織を使用しているため、血栓がつきにくく、ワーファリンが不要となることが長所です。短所としては、10年から15年でカルシウムがついて(石灰化)固くなってしまい、弁が劣化することです。
劣化した生体弁は、再手術が必要となります。以前は再度開胸手術が必要でしたが、大動脈弁に植え込まれた生体弁に限り、条件が揃えば、劣化した生体弁にカテーテル治療(TAVI:経カテーテル的大動脈弁留置術)が可能となっています。
生体弁が劣化して再手術が必要となった場合、カテーテルでの治療の可能性もありますので、ご相談してください。

提供:(株)センチュリーメディカル (図7)

提供:(株)エドワーズライフサイエンス) (図8)
〜人工弁の特徴〜

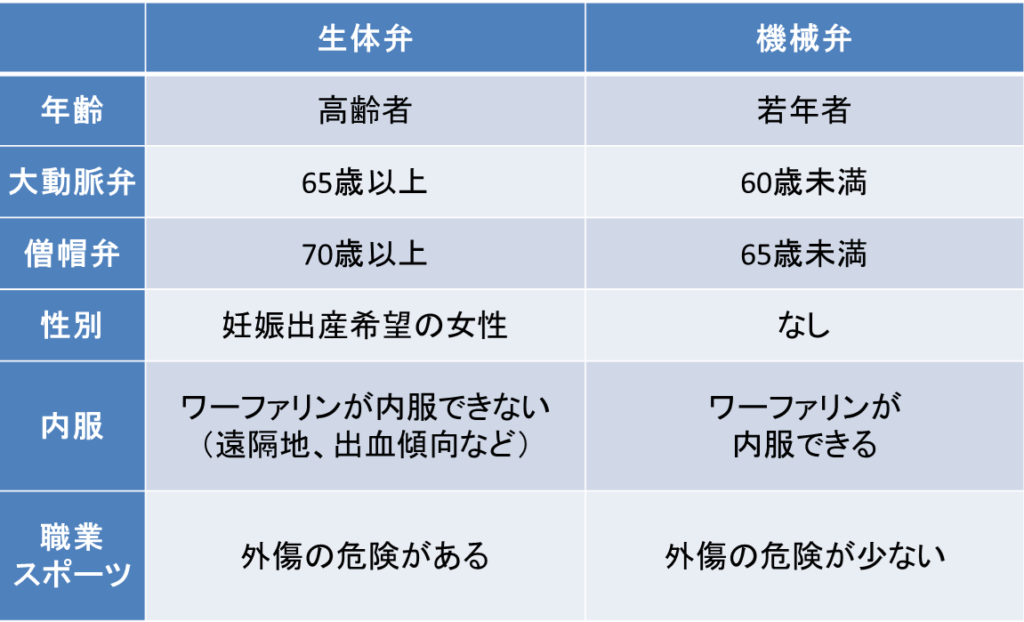
人工弁の選択する基準は、患者様ごとによって異なりますが、通常は年齢で機械弁か生体弁かを選ぶようお勧めしています。
大動脈弁と僧帽弁では生体弁の劣化の程度が異なりますので、大動脈弁では65歳、僧帽弁では70歳以上の高齢者の方には生体弁を、大動脈弁では60歳、僧帽弁では65歳以下の若い方には機械弁をお勧めしています。
ただし、ワーファリン投与を望まない症例(妊娠・出産を控えた女性やアスリートなど)は、若年者であっても生体弁を選択することもあります。患者様ごとの生活スタイルに合わせた人工弁の選択が必要です。
〜人工弁の選択〜
<低侵襲心臓手術(MICS:ミックス)>
心臓は骨(胸骨、背骨、肋骨)に囲まれており、心臓を触ることはできません(図9)。
心臓に到達する一般的な方法として胸の真ん中にある板のような“胸骨”を縦に切る胸骨正中切開法です。心臓手術では最も一般的で、心臓に手が届き、人工心肺装置も心臓の太い血管に管を入れて使用することが可能で、どんな症例にも対応できる優れた方法です。切開した胸骨はワイヤーなどで固定します。胸の真ん中を切開しますので、傷が目立ちやすいことと、胸骨が治るのに2-3ヶ月程度かかってしまい重いものを持ち上げるなど上半身の活動制限がありことが欠点といえます。
そこで胸骨を切開せず、肋骨の間から行う低侵襲心臓手術(MICS:Minimally Invasive Cardiac Surgeryの略、ミックスと読みます)が行われるようになりました。胸の真ん中には傷はなく、美容上とても優れており、胸骨を切らないため上半身の活動制限がなく、早期社会復帰も可能となります。傷の大きさが限られており、心臓までの距離があるため、心臓を直接触ることは難しく、長い手術器具を使用しながら手術を行い、人工心肺装置も心臓の大きな血管に管を入れることができないので、鼠径部(足の付け根)を2〜3cm程度切開して足の付け根の血管から管を入れる必要があります。
現在では3D内視鏡を用いた内視鏡MICSを導入し、カメラを見ながら手術(図10)ができるため、創部が4cm程度(図11)と大きく切開する必要がなくなり、3次元で立体的に心臓や弁の観察も可能になるため、僧帽弁形成術に最も威力を発揮します。
MICSが可能な疾患・症例は1例ごとに異なりますので、ご相談ください。

(図9)


(図10)

(図11)
<大動脈瘤>
心臓から全身に血液を送り出すパイプの役割を果たすのが“大動脈”です。大動脈は脳、消化管、腎臓などの臓器へ向けて多くの枝を出しながら、お臍の下あたりで左右に分かれます。
大動脈瘤とは「大動脈の璧の一部が全周性、局所性に拡大、もしくは突出した状態」になったことをいい、瘤(こぶ)になった状態です。大動脈瘤は、ときに大きくなって周りの臓器への影響(胸部;声が枯れる、食事のつかえ感、腹部;胃部不快感、便秘、腹部鈍痛など)があらわれたり、瘤内の血栓が剥がれて血流障害(脳梗塞、腸梗塞、下肢血流障害)などを起こしたりすることもありますが、多くの場合は無症状で経過します。大動脈瘤の最も大きな問題は、破裂することにあります。大動脈瘤の破裂は突然起こり、血液の通路が破綻するので、大量出血となるため、致命的です。破裂後の致死率は80%以上を超え、救命困難な状態です。
原因:多くの場合は動脈硬化によって起こりますので、半数以上の方に脳の血管(脳梗塞)や心臓の冠動脈にも病気(狭心症や心筋梗塞)を合併しています。
その他には、遺伝的な原因で大動脈の壁が弱くなっている場合や細菌感染がで璧が破壊され起こる場合、外傷性に血管損傷が起こり発症する場合などがあります。
検査:健康診断などで行われるレントゲンや超音波検査では見つけにくい大動脈瘤もあり、確実な診断のためにはCT検査が必要です。
治療の必要性:大動脈瘤は破裂直後に亡くなることも多く、辛うじて病院へ搬送でき緊急手術を行えたとしても、手術死亡率(手術で死亡する確率)は20〜30%です。一方、破裂する前に治療を行えば、手術死亡率は、年齢や合併症などによって子となりますが、一般的に胸部で3〜4%、腹部で1〜2%と低く、破裂する前に治療することが有利であることがわかります。
治療のタイミング:一般的には破裂リスク(危険性)と手術リスクを比較して決めます。大動脈瘤の破裂は、その大きさ、形によって異なり、大きくなるにつれて破裂の危険性は高くなります。一方で手術リスク性は、手術する部位、手術の方法(術式)、患者様の年齢や合併疾患などで決まります。破裂する前に手術が必要ですが、手術も一定の危険性があるため、破裂の危険性が手術の危険性を上回った場合に、治療を検討します。ですので、患者様ごとに治療のタイミングや治療法の選択が異なります。
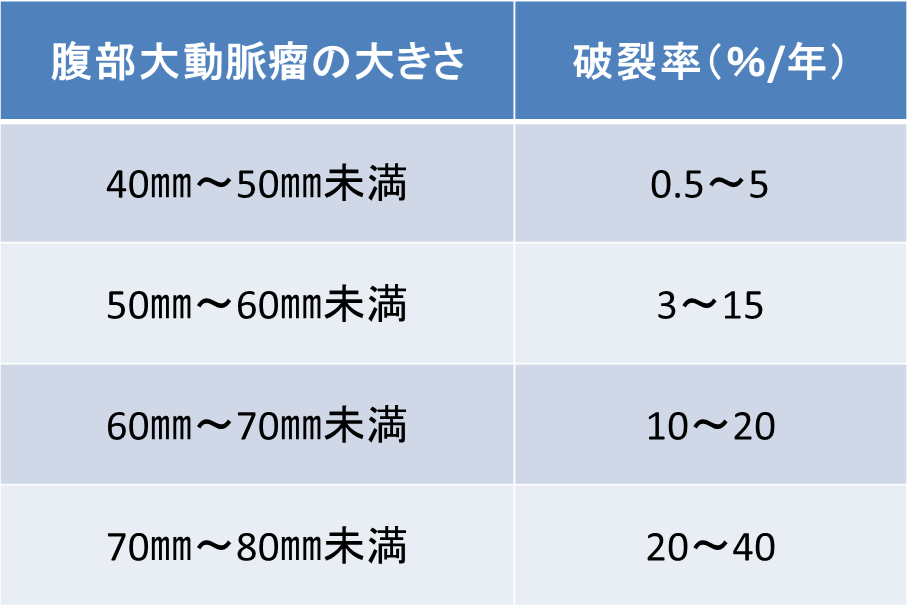
Brewster DC, Cronenwett JL, Hallett JW Jr, et al. Guidelines for the treatment of abdominal aortic aneurysms. Report of a subcommittee of the Joint Council of the American Association for Vascular Sur- gery and Society for Vascular Surgery. J Vasc Surg 2003; 37: 1106- 1117.を改変
大動脈瘤のサイズや全身状態から現時点では手術が必要とならないこともあります。そのような場合も以後の定期検診を忘れてはいけません。大動脈瘤は大きくなればなるほど、拡大スピードが上がります。ゆっくり大きくなったからといって、その後もゆっくり大きくなるわけではありません。ある時、急に拡大することもよく経験します。数年前に、「手術しなくてよいサイズ」と言われた方の大動脈瘤がいつの間にか大きくなって破裂して運ばれてくることも少なくありません。当科では、そのような状態の患者様にも責任を持って観察をさせていただいております。
治療方法:現在のところ、内服薬で治療はできません。大きく2つの治療方法があります。
①人工血管置換術
瘤になっている血管を切除し、人工血管(図13)を使用して、血管を再建する治療方法(図14)
長所:動脈瘤を切除することができる、複雑な動脈瘤の治療も可能
短所:体の負担がカテーテル治療に比べて大きい(開胸、開腹)
術後経過
腹部の場合は術後すぐに人工呼吸器から離脱し翌日には集中治療室を退室となります。痛みがありますが、しっかりと歩行し離床して頂くことが大事です。
胸部の場合は術後数時間で人工呼吸器から離脱できることが多いです。集中治療室も2日程度で退室となります。
どちらも創部など問題ないことを確認し、約7日~14日程度で退院となります。

(図13)
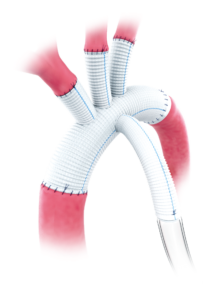

提供:日本ライフライン株式会社 (図14)
②ステントグラフト内挿術
ステントグラフトとは、ステント(バネの形状をした金属)にグラフト(人工血管)が巻き付けてある治療器具です(図15、16)。
大動脈瘤のある部分にステントグラフトを使用して、血管の裏打ち(内挿)し、大動脈瘤にかかる血流を遮断する治療方法
通常足の付け根(大腿動脈)から治療を行い、局所麻酔で行います
長所:体の負担が小さい
短所:大動脈瘤のできる部位や血管の状態によってできない場合がある(重要な血管が近い、血管が曲がっている・細いなど)、再度治療が必要になる場合がある(ステントグラフトと血管との隙間や周囲の血管から大動脈瘤に血流が入って(エンドリーク)大動脈瘤が大きくなることがあるため、定期的にCT検査が必要で、状況によって再治療は開胸・開腹手術が必要になることもあります)、腎臓への負担(造影剤が必要)
術後経過
胸部、腹部どちらも術後合併症がなければ4日程度で退院が可能となります。
1ヵ月後、3か月後、半年後、1年後、各年後とフォローさせて頂き瘤の拡大などを認めれば追加治療が必要となることがあります。
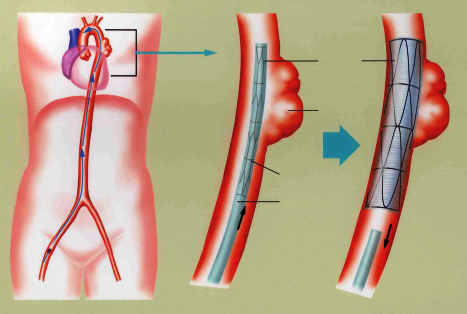
提供:日本ライフライン株式会社

提供:日本ゴア合同会社 (図15)

提供:日本ゴア合同会社 (図16)
ステントグラフト内挿術は長期的な治療成績が不明瞭であるため、開胸・開腹手術が可能である場合は人工血管による手術を第一選択とします。
またステントグラフトと上記の人工血管置換術と組み合わせて治療を行なったり(図17)、人工血管置換術を行った後にステントグラフトを行うこともあります。

提供:日本ライフライン株式会社 (図17)
<不整脈>
当科で治療する不整脈の多くは心房細動です。
心房細動とは、心臓の部屋の一つである心房の中に流れる電気信号の乱れによって起きる不整脈の一種です。心房が痙攣したように細かく震えるため、心房細動と呼ばれます。
心房細動の問題はドキドキするなどの動悸症状、心房の収縮が小さくなり心臓のポンプ機能が低下することが挙げられますが、いちばん問題となるのが、血液の澱みによって心房の中で血液の固まり(血栓)ができ、それが血流に乗って全身に運ばれ、血管を詰まらせてしまうことです。脳に詰まると脳梗塞、腸を栄養する血管に詰まると腸壊死、足に流れる血管が詰まると下肢壊死など、重症な病気を引き起こします。
心房細動となった場合、血栓ができないようにするため、血液が固まりにくくする薬(抗凝固薬)を内服(抗凝固療法)することになります。
不整脈手術
この心房細動を元の正常な脈に戻す治療があり、メイズ手術と言います。心臓の中の、乱れた電気の流れる経路を遮断し、正常な本来の道だけを残すことで正常のリズムにするというものです。この手術で正常な脈に戻った場合、機械弁を使用した場合など特殊な状況を除いて、ワーファリンを止めることができます。
また心房細動の場合、多くは左心房の中にある“左心耳”という部分に血栓ができるといわれています。この部分を切除(閉鎖)することで血栓を作る場所をなくしてしまう手術も同時に行うことができます(左心耳閉鎖術)。
抗凝固療法:心房細動などの血栓ができやすい患者様や機械弁を使用している患者様に行う治療。古くからワーファリンという薬があり、定期的に血液検査をおこなって、容量を調整する必要があります。しかし近年、作用の違いからさまざまな薬剤が選べるようになっています。
*当科の特徴
この不整脈治療も、低侵襲心臓手術(MICS:ミックス)をおこなっております。
特に左心耳の中に既に血栓がある場合は、カテーテル治療ができないため、手術が必要となりますので、一度ご相談ください。
当科も関わるチーム医療
教育体制
学術業績
施設認定
- 心臓血管外科専門医修練施設(基幹施設)、専門医 3
- 日本外科学会外科専門医制度関連施設、 専門医 3
- 胸部ステントグラフト実施施設 実施医 1
- 腹部ステントグラフト実施施設 指導医 1、実施医 1
- 下肢静脈瘤血管内焼灼術実施施設 実施医 3